由于钛及钛合金优异的生物相容性、高比强度及低密度,被认为是具有广泛应用前景的生物医用植入材料, 如髋关节置换, 人造关节、 牙齿等[1-5]。Ti6Al4V合金作为一种应用广泛的钛合金, 尽管其具有高的强度,但是弹性模量也较高,容易产生“应力屏蔽效应”,同时Al和V元素对人体有害,长期存在人体中易引发阿尔兹海默症等疾病[6-9]。因此,这些问题限制了Ti6Al4V合金在生物医疗领域的进一步应用。
近年来, 大量研究表明β型钛合金展示了优异的力学性能, 特别是其弹性模量明显低于α型钛合金[1,3-4,10]。因此,开发β型钛合金作为生物材料将在医疗领域有广泛的应用前景。 众所周知,β相为高温相,为了在常温下获得β相,必须在钛合金中加入一定量的β相稳定元素,如Nb、Mo等,它们在钛合金中不仅能够稳定β相,还可提高合金的力学性能。 Zr元素与Ti元素具有相似的结构与性质, 能够形成无限固溶体, 添加Zr元素也可改善合金的力学性能。 此外,作为生物医用材料,植入人体后优异的耐蚀性能也是非常重要的。 Calderon-Moreno等人[11]报告了Ti-15Zr-10Nb合金在模拟体液中具有优异的耐蚀性;Oliveira等人[12]对Ti-Mo合金的腐蚀行为研究表明其也展示了良好的耐蚀性;Nnamchi等人[13]在Ti-Mo合金中添加了Nb和Zr元素,显著提高了合金的耐蚀性。 这些研究结果表明,Zr、Nb、Mo元素对改善Ti合金在模拟体液中的耐蚀性能是有益的。
本研究制备了Ti-Zr-Nb-Mo合金, 分析了Mo元素对合金的物相结构、显微组织、力学性能及腐蚀性能的影响,为该合金在生物医疗领域的应用提供一定的理论支持。
1 实验材料及方法
选用纯Ti(99.9%)、纯Zr(99.9%)、纯Nb(99.9%)、纯Mo(99.9%)4种元素作为原材料,在非自耗真空钨极电弧熔炼炉中制备Ti-Zr-Nb-Mo合金。为了防止合金发生氧化, 熔炼时保持一定的真空度, 约为8.8×10-4 Pa。 同时,为了使合金的成分更加均匀,在熔炼过程中施加电磁搅拌,电流为5 A,搅拌时长1 min,并重复翻转熔炼5~6次,获得铸态合金样品。
通过机械加工将合金样品切割成规定尺寸,随后进行显微组织及力学性能的检测。采用EPIPHOT 300U 金相显微镜观察合金的显微组织, 借助D/max-2500型X射线衍射仪分析样品的物相, 扫描速度为4°/min。 在CMT5150型电子万能试验机上测试合金的压缩性能,样品尺寸为8 mm×ϕ4 mm,应变速率为1.5×10-4 s-1,选用3个样品。 选用FEM-700硬度计检测合金的显微硬度,载荷200 g,保压时间10 s,每个样品测量10个点取平均值。
采用PARATAT 4000A电化学工作站测试合金的电化学性能,选用三电极体系,氯化银电极为参比电极,铂网为对电极,待测样品为工作电极。 所用的电解质溶液为模拟体液, 成分为NaCl (9 g)+KCl(0.42 g)+CaCl(0.25 g)+H2O(1 L),通过氯化氢和氢氧化钠进行调节,将溶液的pH 调为7.0,溶液的温度为37 ℃, 动电位极化曲线测试的电位为-1.0~1.5V,扫描速率为0.5 mV/s。 测试之前,样品打磨抛光,并超声清洗。
2 结果与讨论
2.1 XRD分析
图1为铸态Ti-Zr-Nb-Mo合金的XRD图谱。 从图中看出,所有样品的衍射峰均为单一的β相,未检测到其它相的衍射峰。 这是由于β相稳定元素Nb和Mo的添加,显著降低了合金β相转变温度,增加了β相的稳定性, 使得合金在水冷铜坩埚中冷却时没有充足的时间发生相变, 最终在室温下获得β相。 此外,随着Mo含量的增加,衍射峰向高角度发生偏移,这是由于Mo元素的原子半径(0.140 nm)明显小于Ti (0.147 nm)、Zr(0.160 nm)和Nb(0.147 nm)元素[14],形成的固溶体晶面间距缩小所致。

图1 铸态Ti-Zr-Nb-Mo 合金的XRD 图谱
Fig.1 XRD patterns of as-cast Ti-Zr-Nb-Mo alloys
2.2 显微组织
图2 为铸态Ti-Zr-Nb-Mo合金的光学显微组织。从图中看出,粗大的β晶粒清晰可见,未观察到其它相,这与XRD的分析结果相一致。随着Mo元素从8%增加15%,合金的平均晶粒尺寸先减小后增大,分别为152、53、118和180 μm,铸态(TiZr)80Nb10Mo10合金的平均晶粒尺寸最小,表明添加一定量的Mo元素可以细化合金的晶粒尺寸。这是由于在铸态Ti-Zr-Nb-Mo合金中添加一定量的Mo元素导致成分过冷, 当Mo含量从8%增加到10%时, 固溶的Mo元素促进了合金中的形核,使得晶粒细化;当添加Mo元素超过13%后, 过量的Mo使得合金中的非均匀形核降低,导致合金的晶粒尺寸增大。 这一现象在Ti-Zr-B合金中也被发现[15]。

图2 铸态Ti-Zr-Nb-Mo 合金的显微组织
Fig.2 Microstructure of as-cast Ti-Zr-Nb-Mo alloys
2.3 力学性能
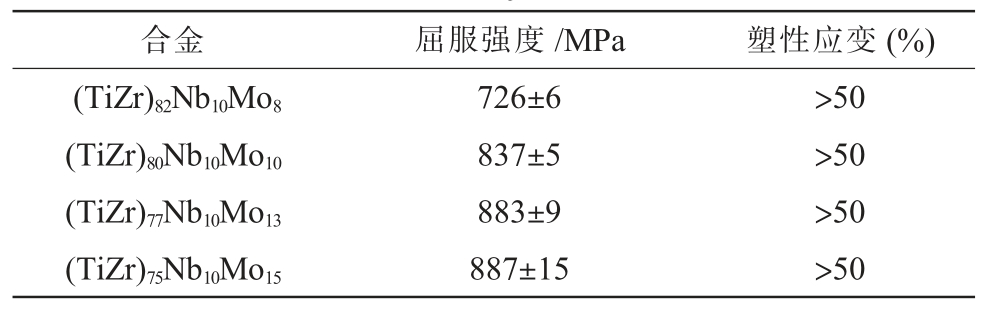
图3为铸态Ti-Zr-Nb-Mo合金的室温压缩应力应变曲线。表1列出了合金压缩性能的数据。从表中可以看出,随着Mo含量从8%增加到15%,合金的屈服强度(σ0.2)显著增大,从726 MPa增加到887 MPa,提高了22%。 合金强度的提高,主要是由于Mo元素与合金形成固溶体,使晶格发生畸变,产生固溶强化,Mo元素越多,合金的晶格发生畸变越严重,固溶强化效果越显著,合金的强度越高。 根据合金的显微组织及细晶强化理论,Mo含量超过13%后, 合金的晶粒尺寸明显增大,但合金的强度并未降低,这是由于固溶强化在合金中占有主导地位所致。 在塑性变形阶段,随着应变的增加,合金的应力显著提高,发生了形变强化,应变超过50%,样品仍未压断,展示了良好的塑性。
表1 铸态Ti-Zr-Nb-Mo合金的力学性能
Tab.1 The mechanical properties of as-cast Ti-Zr-Nb-Mo alloys
?
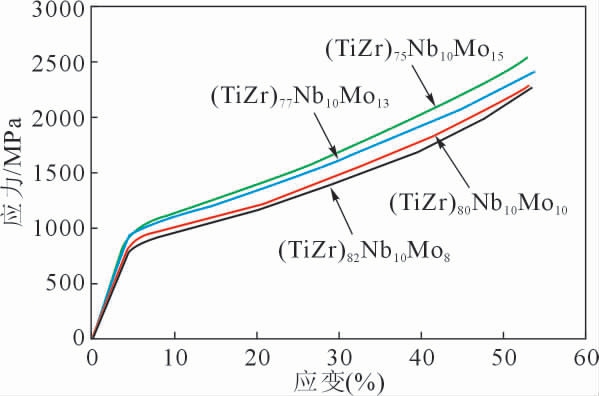
图3 铸态Ti-Zr-Nb-Mo 合金的压缩应力应变曲线
Fig.3 Compressive stress-strain curves of as-cast Ti-Zr-Nb-Mo alloys
图4 为铸态Ti-Zr-Nb-Mo合金的硬度柱状图。 从图中看出,随着Mo含量的增加,合金的硬度也显著增加。 当Mo含量为8%时,合金的硬度为379 HV;当Mo元素添加量为15%时,硬度增加到471 HV,提高了24%。 合金硬度的增加主要是由于固溶强化和细晶强化所致,其中固溶强化起主导所用。这与合金强度的变化相一致。

图4 铸态Ti-Zr-Nb-Mo 合金的硬度随Mo 含量的变化
Fig.4 Variation of hardness of as cast Ti-Zr-Nb-Mo alloys with Mo content
2.4 腐蚀性能
图5为铸态Ti-Zr-Nb-Mo合金在模拟体液中的动电位极化曲线。从图中可以看出,所有合金样品在阳极区均有一水平直线段,随着电位升高,电流密度维持不变,这表明在合金表面形成了钝化膜,产生钝化。 随着电位继续增加,钝化膜被击穿,腐蚀电流密度增加。 自腐蚀电位和自腐蚀电流密度是评估材料耐蚀性的两个重要参数,自腐蚀电位越大,自腐蚀电流密度越小,材料的耐蚀性越好[16]。 从极化曲线中获得的腐蚀数据见表见2。合金的自腐蚀电位为-324.6~-348.8 mV,自腐蚀电流密度为692.2~786.4 nA·cm-2, 其中,(ZrTi)80Nb10Mo10合金的自腐蚀电位最大, 且其自腐蚀电流密度最小,所以,(ZrTi)80Nb10Mo10合金在模拟体液中的耐蚀性最好。 材料发生腐蚀也是其表面失效的一种,主要与材料的相组成、晶粒尺寸、表面粗糙度等因素有关。所有Ti-Zr-Nb-Mo合金的相均为单一的β相,且其表面用相同型号的砂纸进行了打磨,因此, 相组成和粗糙度对合金腐蚀性能的影响可以忽略。 从图2中可知,随着Mo含量的增加,合金的平均晶粒尺寸是先减小再增大,(ZrTi)80Nb10Mo10合金的平均晶粒尺寸最小。 研究表明,晶粒尺寸对合金的腐蚀性能有明显的影响,细化晶粒可以提升晶界处的电化学活性, 促使钝化膜在材料表面快速产生,形成保护膜提高耐蚀性[17]。 所以,(ZrTi)80Nb10Mo10合金具有最佳的耐蚀性。

图5 铸态Ti-Zr-Nb-Mo 合金在模拟体液中的动电位极化曲线
Fig.5 The potentiodynamic polarization curves for as-cast Ti-Zr-Nb-Mo alloys
表2 铸态Ti-Zr-Nb-Mo合金的腐蚀数据
Tab.2 Corrosion datas of as-cast Ti-Zr-Nb-Mo alloys

?
3 结论
(1)通过真空熔炼炉制备了不同成分的Ti-Zr-Nb-Mo合金,其均为单一的β相,随着Mo含量的增加,衍射峰向高角度发生偏移。
(2)当Mo元素从8%增加到15%时,合金的平均晶粒尺寸先减小再增大,铸态(TiZr)80Nb10Mo10合金的平均晶粒尺寸最小。
(3)随着Mo含量的增加,合金的强度和硬度显著提高,铸态(TiZr)75Nb10Mo15合金的屈服强度和硬度最高,分别为887 MPa和471 HV。 铸态(ZrTi)80Nb10Mo10合金的自腐蚀电位为-261.1 mV,自腐蚀电流密度为354.5 nA·cm-2,耐蚀性最好。
[1] GEETHA M, SINGH A K, ASOKAMANI R, et al. Ti based biomaterials,the ultimate choice for orthopedic implants-a review[J].Progress in Materials Science,2009,54:259-264.
[2] CHEN Q,THOUAS G A.Metallic implant biomaterials[J].Materials Science and Engineering:R:Reports,2015,87:1-57.
[3] ZHANG L C,CHEN L Y.A review on biomedical titanium alloys:recent progressand prospect[J]. Advanced Engineering Materials,2019,21:1801215.
[4] LI Y H, YANG C, ZHAO H D, et al. New developments of Ti based alloys for biomedical applications[J]. Materials, 2014, 7:1709-1800.
[5] 余挺,王晓蓉,于连旭,等. 钛合金低成本化制备技术研究现状[J].铸造技术,2021,42(1):61-64.
[6] OKAZAKI Y.Effect of friction on anodic polarization properties of metallic biomaterials[J].Biomaterials,2002,23:2071-2077.
[7] LOPEZ M F, JIMENEZ J A, GUTIERREZ A. Corrosion study of surface-modified vanadium-free titanium alloys[J].Electrochimica Acta,2003,48:1395-1401.
[8] MCLACHLAN D R C. Aluminium and the risk for Alzheimer’s disease[J].Environmetrics,1995,6:233-275.
[9] RAO S, USHIDA T, OKAZAKI Y, et al. Effect of Ti, Al, and V ions on the relative growth rate of fibroblasts (L929) and osteoblasts (MC3T3-E1) cells[J].Bio-medical Materials and Engineering,1996,6:79-86.
[10] LIU Y J,LI S J, ZHANG L C, et al. Early plastic deformation behavior and energy absorption in porous β-type biomedical titanium produced by selective laser melting[J]. Scripta Materialia, 2018,153:99-103.
[11] CALDERON—MORENOJM J M, VASILESCU C, DROB S I, et al.Microstructural and mechanical properties,surface and electrochemical characterisation of a new Ti-Zr-Nb alloy for implant applications [J]. Journal of Alloys and Compounds, 2014, 612:398-410.
[12] OLIVEIRA N T C,ALEIXO G,CARAM R,et al.Development of Ti-Mo alloys for biomedical applications:microstructure and electrochemical characterization[J]. Materials Science and Engineering:A,2007,452-453:727-731.
[13] NNAMCHI P S,OBAYI C S,TODD I,et al.Mechanical and electrochemical characterisation of new Ti-Mo-Nb-Zr alloys for biomedical applications[J].Journal of the Mechanical Behavior of Biomedical Materials,2016,60:68-77.
[14] BIESIEKIERSKI A, PING D, LI Y, et al. Extraordinary high strength Ti-Zr-Ta alloys through nanoscaled, dual-cubic spinodal reinforcement[J].Acta Biomaterialia,2017,53:549-558.
[15] CHUI P F.Effect of boron content on microstructure and mechanical properties of Ti50Zr50 alloys[J].Vacuum,2018,154:25-31.
[16] 炊鹏飞,董洪峰,景然,等. 退火处理对表面纳米化316L 不锈钢组织及耐腐蚀性能的影响[J]. 材料热处理学报,2019,40(12):144-149.
[17] LI D Y.Electron work function at grain boundary and the corrosion behavior of nanocrystalline metallic materials[C].MRS Proceedings,2006,887:227-235.